Sehr geehrte Kolleginnen und Kollegen,
die Analyte Parathormon-related Peptid (PTHrP), Vasoaktives intestinales Peptid (VIP) und Glukaogon (GLUK) sind präanalytisch sehr instabil.
Um valide Resultate zu erhalten, hat der Testhersteller seine Vorgaben zur Präanalytik verschärft.
Ab dem 1. März 2026 kann die Analyse nur noch aus gefrorenem Aprotinin-stabilisiertem
EDTA-Plasma durchgeführt werden.
Diese speziellen Röhrchen für die Blutentnahme können Sie bei uns bestellen. Durch den enthaltenen
Zusatz Aprotinin wird der Abbau von genannten Parametern inhibiert und der Analyt stabilisiert.
Die Blutprobe muss spätestens 2 Stunden nach der Entnahme zentrifugiert werden, das Plasma
abgenommen und tiefgefroren werden. Danach kann das Plasma bei –20°C bis zu 4 Wochen
gelagert und transportiert werden.
Für weitere Fragen stehen wir Ihnen gerne zur Verfügung:
Dr. rer. nat. Sylvia Schön Tel. 05222 8076-159
Mit freundlichen Grüßen
Ihr Labor Krone


Liebe Neurologinnen und Neurologen,
wir freuen uns, Ihnen in Kooperation mit unserem Partnerlabor die Bestimmung des Demenzmarkers
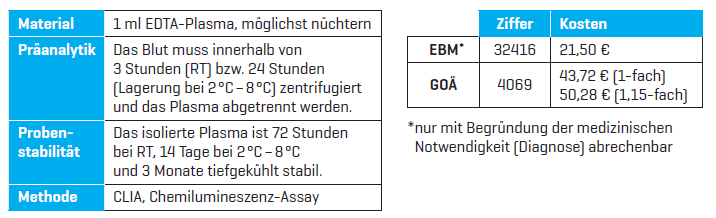
pTau217 im Plasma anbieten zu können. Damit ergibt sich die Möglichkeit einer minimalinvasiven Labordiagnostik zur Abklärung einer Alzheimer-Demenz bereits in einem frühen Stadium der Erkrankung und es eröffnen sich neue Perspektiven für Diagnostik, Prognose und Therapie-Monitoring.
pTau217 ist eine (an Threonin 217) phosphorylierte Tau-Variante, die auch im Plasma zuverlässig messbar
ist. Sie spiegelt aufgrund ihrer engen Korrelation mit der Amyloid- und der Tau-Pathologie im Liquor die
Alzheimer-Demenz im Plasma mit hoher krankheitsspezifischer Aussagekraft wider und erlaubt eine gute
Differenzierung der Alzheimer-Krankheit gegenüber anderen neurodegenerativen Erkrankungen.
Hinweis: Dieser Test sollte nicht für ein flächendeckendes Screening asymptomatischer Personen, sondern
zur gezielten Abklärung einer (milden) kognitiven Beeinträchtigung mit Verdacht auf eine Alzheimer-
Demenz angewendet werden. Die Entscheidung zur Testdurchführung sollte in enger Abstimmung mit
neurologischen Fachärztinnen und Fachärzten erfolgen.
Die Beurteilung der pTau217-Konzentrationen sind von Einflussgrößen wie Alter, Geschlecht, BMI, Nierenfunktionund anderen Grunderkrankungen wie Apoplex und Myokardinfarkt abhängig und müssen immer im Zusammenhang mit weiteren Befunden bewertet werden. Die Entscheidungsgrenzen gelten nur für nierengesunde Patienten!
Für weitere Fragen stehen wir Ihnen gerne zur Verfügung:
Dr. rer. nat. Sylvia Schön Tel. 05222 8076-159
Jasmin Steube, M.Sc. Tel. 05222 8076-476
Mit freundlichen Grüßen
Ihr Labor Krone

November 2025
Sehr geehrte Kolleginnen und Kollegen,
der Reagenzienhersteller Roche hat uns auf folgenden Sachverhalt hingewiesen:
Unter Verwendung der von Roche in Umlauf gebrachten Reagenzien ist es zu Fehlbestimmungen der TRAK-Auto-Antikörper gekommen. D.h. die von unserem Labor im Zeitraum vom 20.02.2025 bis zum 24.11.2025 erhobenen gemessenen Werte im Grenzwertbereich können um bis zu ca. 50% falsch zu niedrig gemessen worden sein.
Mit Erreichen dieser Nachricht haben wir die Analytik unverzüglich auf eine nicht betroffene Reagenziencharge umgestellt. Als weitere Maßnahme haben wir einen groben Vergleich der TRAK-Konzentrationen mit Vorbefunden, TSH-Spiegeln sowie von fT3 und fT4 vorgenommen, ohne dass wir auf ersichtliche Diskrepanzen gestoßen sind.
Sollten Ihnen allerdings im Zusammenhang mit den klinischen Daten Unregelmäßigkeiten auffallen, wird eine Kontrollmessung empfohlen.
Wichtige Korrekturmaßnahme: Abweichungen des Elecsys® Anti-TSHR bei cobas® e 411,
cobas® e 402 und cobas® e 801 (Referenz: RDS-CoreLab-2025-004)
Mit freundlichen Grüßen
Ihr Labor Krone

Sehr geehrte Kolleginnen und Kollegen,
gern informieren wir Sie über die neuen Möglichkeiten der modernen Allergie-Diagnostik im Labor Krone.
Rund 90% aller Allergien zählen zum Soforttyp, auch Typ-I-Allergie genannt, bei dem die Reaktion unmittelbar nach Allergenkontakt einsetzt. Diese schnelle Immunantwort wird durch IgE-Antikörper gegen das Allergen vermittelt.
Auslöser erkennen
Die Suche nach dem allergieauslösenden Stoff kann mit einzelnen Hauttests und Blutuntersuchungen auf einzelne Allergene sehr langwierig sein. Besonders wenn man unter allergischen Symptomen wie laufende Nase, juckende Augen, Husten, Atembeschwerden und Hautausschlägen leidet, aber keinen konkreten Verdacht hat, welches Allergen die Symptome auslöst. Und auch bei mehrfach sensibilisierten Personen ist es oft schwierig, den konkreten Auslöser zu finden.
Allergen-Screening
In Fällen ohne konkreten Verdacht liefert ein umfassendes Allergen-Screening ein detailliertes Sensibilisierungsprofil. Der innovative Allergietest ALEX2® Allergy Explorer misst spezifische IgE-Antikörper von 295 potenziellen Allergieauslösern in nur 1 ml Blut (Serum). Damit deckt er 99% der möglichen Typ-I-Allergenquellen ab. Der Test identifiziert dabei nicht nur die Allergieauslöser, sondern liefert auch Hinweise auf Kreuzallergien und dem Risiko einer anaphylaktischen Reaktion.
Die Krankheitsgeschichte (Anamnese) und eine Untersuchung der Patientin/des Patienten sind die ersten Schritte einer Allergiediagnose. Für das Allergen-Screening wird in der Arztpraxis dann eine Blutprobe entnommen und zur Analyse in das Labor geschickt. Das Laborergebnis wird einem verständlichen Laborbericht mit diagnostischer Beurteilung übermittelt.

Allergiediagnostik als Wunschleistung
Allergiediagnostik als Vorsorge gehört in der Regel nicht zu den Leistungen der gesetzlichen Krankenkassen und muss gegebenenfalls vom Patienten/der Patientin selbst übernommen werden. Weiterführende Untersuchungen bei Bestätigung einer Verdachtsdiagnose werden von den Kassen in begrenztem Umfang bezahlt. Das Allergen-Screening mit dem ALEX2® Allergy Explorer ist eine individuelle Gesundheitsleistung (IGeL) und wird nicht von den gesetzlichen Krankenkassen übernommen.
Mit freundlichen Grüßen
Ihr Labor Krone

Sehr geehrte Kolleginnen und Kollegen,
gern möchten wir Sie auf die aktuellen Publikationen im Bereich der Neuralen Antikörper aufmerksam machen:
Zum Thema „Temporallappenepilepsie und GAD-Antiköper“ ist von Herrn Prof. Dr. Christian Bien in dem renommierten Journal „Neurology Neuroimmunology Neuroinflammation“ ein Artikel erschienen, der die GAD-Antikörper-assoziierte Temporallappenepilepsie als neues epilepsie-Syndrom beschreibt und auch unsere Labormethoden zur Diagnostik dieser Antikörper erläutert .
Erschienen in: Rada A et al. Neurol Neuroimmunol Neuroinflamm 2025;12(4):e200422.
Weitere relevante Artikel finden sich zu folgenden Themen:
Anti-AMPA Receptor Encephalitis: In der retrospektiven, internationalen Kollaborationsstudie wurden ausgeprägte, klinisch-radiologische Merkmale bei Kindern und Erwachsenen mit Anti-AMPA-Enzephalitis gezeigt. Bei einem Beobachtungszeitraum von über 24 Monaten, wurden bei 68% der untersuchten Patienten – alles Erwachsene – neurologgische Folgeerscheinungen erkannt, wobei die Resultate dramatischer sind, wenn Patienten nicht auf first-line Immuntherapie ansprechen.
Erschienen in: Milano C et al. Neurol Nweuroimmunol Neuroinflamm 2025;12(5):e200453
Autoimmune encephalitis-associated epilepsy: In der Übersichtsarbeit wird eine Untergruppe der Autoimmun-Enzephalitis beleuchtet, die aufgrund eines gemeinsamen Mechanismus der strukturellen Schädigung und Beteiligung von zytotoxischen T-Zellen resistent gegen Immuntherapie sind. Das neue Konzept der Autoimmun enzephalitis-assoziierten Epilepsie (AEAE) wird anhand klinischer Charakteristika verdeutlicht und erforderliche Änderungen in der Diagnostik und Therapie disktutiert.
Erschienen in: Steriade C et al. Nat Rev Neurol. 2025 Jun;21(6):312-326
LGI1 encephalitis: Zwei Drittel der Patienten mit einer LGI1-Ezephalitis (anti-leucine rich, glioma inactivated 1 (LGI1) encephalitis) entwickeln eine Hippokampusatrophie – Abnahme des Hippokampusvolumens, Absterben von Neuronen und reaktive Veränderung von Gliazellen. Die retrospektive Untersuchung von Antikörper- und MRT-Daten zeigt eine Korrelation der Hippokampusatrophie mit den LGI1-Antikörper Subklassen 1 – 3, die zusätzlich zur Subklasse 4 in diesem Krankheitsbild auftauchen.
Erschienen in: Bien CG et al. J Neurol 2024 Aug;271: 6325–6335

Sehr geehrte Damen und Herren,
wir möchten Sie gerne auf unsere neue Diagnostik zur KIR- und HLA-C Genotypisierung im Kontext von unerfülltem Kinderwunsch, Implantationsversagen oder Fehlgeburten hinweisen. Die Interaktion der Killerzell-Immunglobulin-like-Rezeptoren (KIR) in den uterinen NK-Zellen und HLA-C Antigenen des Embryos können eine Rolle bei verschiedenen Schwangerschaftskomplikationen spielen. Mit der angebotenen KIR Genotypisierung wird untersucht, ob bei der Frau ein KIR Genotyp vorliegt (AA), der mitursächlich für den unerfüllten Kinderwunsch sein kann. In Kombination mit dem HLA-C Genotyp kann so eine mögliche Erklärung für den unerfüllten Kinderwunsch und ein neuer Ausgangspunkt für eine Kinderwunschbehandlung gefunden werden.
Nach Analyse der 16 KIR-Gene wird der sich daraus ergebenden KIR-Genotyp (AA oder Bx) ermittelt. Eine HLA-C Genotypisierung kann als Stufendiagnostik oder gleichzeitig angefordert werden. Für den möglichen Vater kann eine HLA-C Analyse als eigener Auftrag ebenfalls sinnvoll sein, v.a. wenn bei der Partnerin der KIR Genotyp AA vorliegt.
Anforderungsschein
Für diese genetische Diagnostik wird eine Einwilligungs-Erklärung gemäß Gendiagnostikgesetz benötigt. Bitte verwenden Sie für die Anforderung einen auf unserer Website verlinkten Humangenetik Anforderungsschein.
Anforderungstext
KIR- und HLA-C-Genotypisierung (wenn gewünscht Stufendiagnostik angeben)
Abrechnung
Nur als Selbstzahlerleistung möglich:
KIR Genotypisierung: 241,33 €
HLA-C Genotypisierung: 227,91 €
Probenmaterial
3 ml EDTA Blut
Für weitere Fragen stehen wir Ihnen gerne zur Verfügung:
Dr. rer. nat. Christina Winkler und Dr. rer. nat. Christiane Walter Tel. 05222 8076-460
Mit freundlichen Grüßen
Ihr Labor Krone

Liebe Neurologinnen, liebe Neurologen,
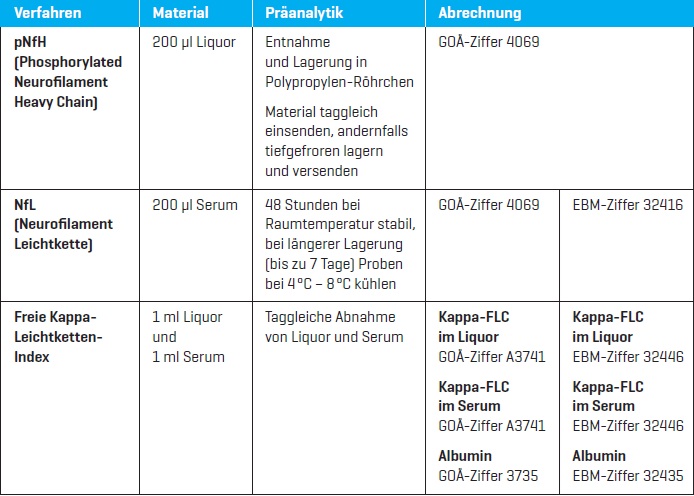
wir haben die Analytik der Neurofilamente im Serum von der phosphorylierten Neurofilament-
Schwerkette (pNfH) auf die Bestimmung der Neurofilament-Leichtkette (sNfL) geändert. Neben
einer höheren Sensitivität verfügt dieser Assay über eine robustere Präanalytik. Die sNfLs sind für
48 Stunden bei Raumtemperatur stabil, bei längerer Lagerung (bis zu 7 Tage) müssen die Proben bei
4°C– 8°C gekühlt werden.
Die Neurofilament-Leichtkette ist das am häufigsten vorkommende Intermediärfilament im ZNS.
Als Biomarker spiegeln erhöhte sNfL akute neuroaxonale Schädigungen im ZNS, wie z. B. bei
Multipler Sklerose (MS), Amyotropher Lateralsklerose (ALS), Demenz, Creutzfeldt-Jakob-Krankheit,
Schädel-Hirn-Trauma etc. wider.
Der besondere Aspekt ist die Bestimmung der sNfLs bei Multipler Sklerose; der hochsensitive
Immunoassay ermöglicht eine spezifische Quantifizierung und erlaubt somit das Erkennen einer
Krankheitsaktivität, bevor diese im MRT sichtbar wird. Die Veränderungen der sNfL-Werte korrelieren
mit der MS-Krankheitsaktivität (sNfL-Anstieg) und Therapieansprechen (sNfL-Reduktion).
Die NfL-Spiegel im Serum sind u. a. abhängig vom Alter; der altersabhängige Anstieg
beträgt etwa 2,5% pro Jahr.
Unverändert bestimmen wir weiterhin die phosphorylierten Neurofilament-Schwerketten
(pNfH) im Liquor sowie den Freie Kappa-Leichtketten-Index.
Die Bestimmung von NfL ist bei der schubförmig verlaufenden MS eine Regelleistung.
Im Rahmen dieser Anpassung haben wir unseren Neurodiagnostikum Anforderungsschein 2
überarbeitet. Wir bitten um Verwendung des neuen Einsendescheins, den Sie direkt von unserer
Homepage ausdrucken können.
Für weitere Fragen stehen wir Ihnen gerne zur Verfügung:
Jasmin Steube, M. Sc. Tel. 05222 8076-476
Dr. rer. nat. Sylvia Schön Tel. 05222 8076-159
Mit freundlichen Grüßen
Ihr Labor Krone

Sehr geehrte Damen und Herren,
wir möchten Sie gerne auf unsere Diagnostik zum Nachweis von Respirationstrakterregern mittels PCR-Verfahren hinweisen.
Mit unserem an die heutigen Erfordernisse angepassten Multiplex-PCR-Test können 26 relevante virale und bakterielle Erreger bzw. Subtypen gleichzeitig aus einer Probe nachgewiesen werden.
Bei Bedarf zur Klärung weiterer Fragen stehen wir Ihnen jederzeit gerne zur Verfügung.
Anforderungsschein
Überweisungsschein Ü10 oder Ü10 mit Anhang
Anforderungstext: »Respi-PCR«
Abrechnung
EBM im Verdachtsfall*
IGeL
SARS-CoV-2 + Influenza + RSV 33,52€
SARS-CoV-2 + Respi-Multiplex 67,02€
*Ausnahmeziffer 32006 bei Verdacht auf meldepflichtige Erkrankungen
Probenmaterial
(1 ml Material bzw. 1– 2 Abstriche)
• Nasalabstrich /-spülung
• Nasopharyngealabstrich / -aspirat
• Rachenabstrich
• Trachealsekret / -aspirat
• Bronchiallavage (BAL)
• Sputum
• andere Materialien nach Rücksprache
Erregerspektrum (Multiplex-PCR)
SARS-CoV-2 Virus
Influenza A Virus
Influenza B Virus
RSV (Respiratorisches Synzytial-Virus)
Adenovirus (AdV)
Enterovirus (HEV)
Parainfluenza virus 1 (PIV 1)
Parainfluenza virus 2 (PIV 2)
Parainfluenza virus 3 (PIV 3)
Parainfluenza virus 4 (PIV 4)
Metapneumovirus (MPV)
Bocavirus (HBoV)
Rhinovirus (HRV)
Coronavirus NL63 (CoV NL63)
Coronavirus 229E (CoV 229E)
Coronavirus OC43 (CoV OC43)
Legionella pneumophila (LP)
Haemophilus influenzae (HI)
Streptococcus pneumoniae (SP)


